去年,美国一名10个月大的婴儿通过CRISPR基因编辑技术治愈罕见遗传病,成为全球首例。不过,CRISPR在更广泛遗传病治疗中的推广仍受限于稳定性问题,以及对健康基因造成潜在损害的风险。
CRISPR常被称为“基因剪刀”,可用于对有缺陷基因进行剪切、移除与替换。与此同时,该技术也存在已知安全隐患:相关活性酶可能在细胞内残留,进而对DNA或RNA造成非预期损伤,即“脱靶效应”,并可能引发健康基因的有害突变。
在这一背景下,抗CRISPR蛋白被视为控制并规范CRISPR机制的重要工具。这类蛋白源自感染细菌的病毒,能够抑制CRISPR活性,但其数量稀少且难以发现。
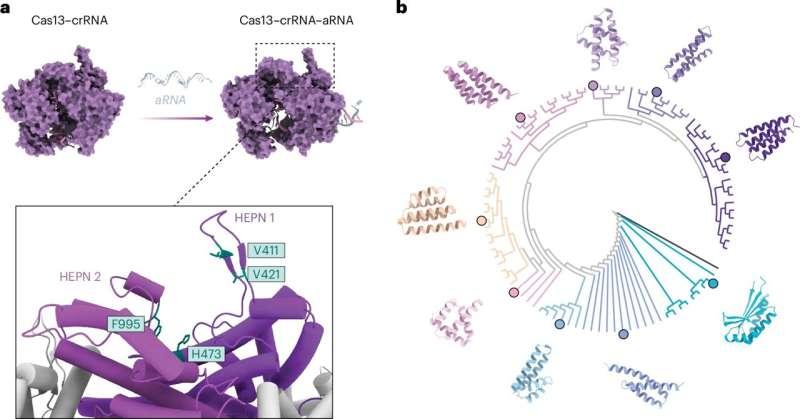
莫纳什大学生物医学发现研究所加文·诺特(Gavin Knott)副教授团队与墨尔本大学Bio21分子科学与生物技术研究所的D. Rhys Grinter合作,在《自然化学生物学》期刊发表研究,介绍了一种借助人工智能实现的高效、快速抗CRISPR分子设计方法。
论文第一作者、莫纳什大学蛋白质设计师辛蒂娅·塔韦诺(Cynthia Taverner)博士表示,研究团队通过人工智能加速的蛋白质设计,快速生成了可在细菌与人类细胞中发挥作用的CRISPR抑制剂。
诺特称,具备设计定制抑制剂以规范CRISPR的能力,将推动CRISPR工具在科研、医学、农业与微生物学等领域的持续发展。
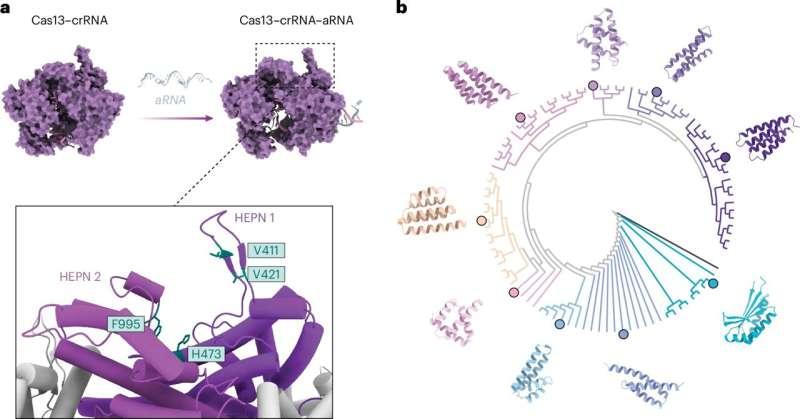
研究人员指出,过去十年的CRISPR研究中仅鉴定出118种抗CRISPR分子。Grinter表示,针对临床相关靶点寻找天然抑制剂仍然具有挑战性且耗时。
据介绍,该研究提出的快速设计方法利用人工智能生成高度精准且具特异性的抗CRISPR分子,本次研究聚焦于对RNA编辑酶活性的控制。研究团队称,新流程较传统蛋白质发现路径更为快捷,从靶点选择到命中与先导分子鉴定仅需8周,有望加快面向临床应用的开发进程。











