mRNA疫苗接种后常见的疼痛、轻微发热和全身不适等反应,通常在数日内缓解,被认为与免疫系统被激活有关。宾夕法尼亚大学研究人员在《自然材料》(Nature Materials)发表研究称,他们通过改造mRNA新冠疫苗常用递送载体脂质纳米颗粒(LNPs)的关键组成,在人体细胞与小鼠模型的临床前测试中,实现了与现有商业配方相当的疫苗表现,同时降低与炎症相关的指标。
研究团队将改造重点放在LNPs核心成分“可电离脂质”的结构上。论文称,这一化学层面的调整一方面增强了关键免疫细胞的代谢能力,为免疫应答提供能量;另一方面降低了与发热、疲劳等反应相关的炎症信号,并提升了纳米颗粒向淋巴结等免疫器官的靶向递送。
论文资深作者、宾夕法尼亚大学生物工程副教授Michael J. Mitchell表示,这项工作仍处于早期阶段,但为开发更有效且耐受性更好的新一代mRNA疫苗提供了可能。
从“递送载体”到“代谢调节”
研究人员指出,LNPs长期以来主要被视为将遗传指令等治疗物质送入细胞的载体,而该研究显示,LNPs的化学组成也可能影响免疫细胞代谢,从而改变mRNA疫苗的整体效果。

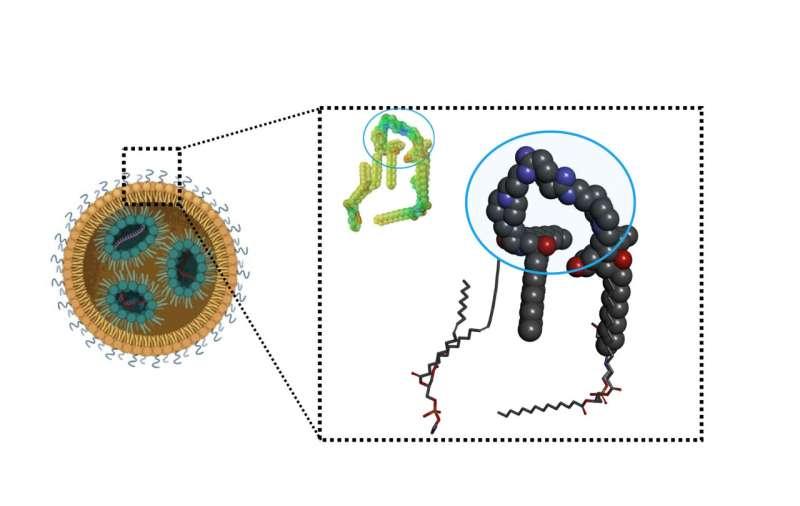
研究共同第一作者、宾夕法尼亚大学生物工程博士后Dongyoon Kim介绍,团队在标准脂质配方基础上引入亚胺酯交联剂,以扩展可电离脂质结构设计空间。研究中表现最佳的脂质被命名为C12-2aN(按其化学结构命名)。
研究称,含C12-2aN的LNPs可增强树突状细胞代谢。树突状细胞在疫苗接种后参与引导免疫系统识别病毒或病原体。Kim将其比作“发动机”,认为当免疫细胞进入防御状态时,会调整能量来源。

在人体树突状细胞与小鼠模型中,含C12-2aN的LNPs提高了与糖酵解相关基因的表达,并伴随乳酸产量增加。研究同时指出,这种代谢提升并未削弱疫苗表现:在mRNA新冠疫苗小鼠模型中,重新设计的脂质与美国食品药品监督管理局(FDA)批准配方的表现相当。
炎症相关指标下降
研究人员表示,疫苗免疫激活往往伴随炎症分子释放,这有助于协调免疫反应,但也可能带来发热、疲劳等不适。该研究认为,新脂质在增强免疫细胞能量供给的同时,使免疫激活更受控并更集中于免疫细胞。

Mitchell实验室博士生、研究共同作者Amanda Murray称,树突状细胞获得发起保护性疫苗反应所需能量的同时,并未触发通常与接种后不适相关的广泛炎症水平。
与FDA批准的可电离脂质相比,研究称含C12-2aN的LNPs在人类细胞与小鼠中降低了与系统性炎症相关基因的表达,并减少小鼠血液中的炎症标志物水平;在体温变化方面,使用重新设计脂质的小鼠体温升高幅度也更小。


向淋巴结递送增强
研究还关注LNPs的非靶向递送问题。论文指出,纳米颗粒常更易在肝脏聚集,而非免疫反应协调所需的淋巴器官。研究称,采用C12-2aN后,LNPs在改善代谢与降低系统性炎症的同时,也提升了靶向递送能力。
研究数据显示,与FDA批准配方相比,重新设计的LNPs递送至淋巴结的mRNA量为肝脏的三倍以上。Kim表示,新成分带来的正电荷可能影响颗粒与组织及蛋白质的相互作用,从而提高其到达目标组织的概率。
后续研究方向
研究团队表示,尽管本研究重点聚焦树突状细胞,但他们也观察到脂质化学变化可促进其他免疫细胞的糖酵解,提示工程化可电离脂质或可用于调节癌症、自身免疫及其他免疫介导疾病相关的免疫细胞代谢。Mitchell称,该研究显示脂质化学设计不仅可能改善递送,也可能用于有目的地塑造免疫细胞代谢,为疫苗之外的免疫工程应用提供路径。











