近年来,mRNA脂质纳米颗粒(mRNA–LNPs)被视为多种疾病治疗的重要递送平台,应用场景涵盖COVID-19、多类癌症及慢性遗传性疾病。不过,该技术此前尚未在胰腺相关疾病上实现有效递送。中国科学家近日在《自然》杂志发表论文,报告一种面向胰腺设计的新型脂质纳米颗粒递送系统。
胰腺递送的关键障碍
脂质纳米颗粒是一类脂肪基载体,可包裹并将信使RNA等核酸递送入细胞。研究团队指出,既往LNPs难以用于胰腺的重要原因在于其在体内往往自然富集于肝脏和脾脏,导致治疗分子在胰腺难以达到足够浓度。
研究人员进一步观察到,肝脏和脾脏外层存在致密的保护性外膜(包膜),而胰腺仅由较薄的结缔组织覆盖。团队据此提出假设:器官包膜可能充当“生物过滤器”。在这一思路下,若将纳米颗粒设计得足够大,或可被肝脏与脾脏的包膜在物理层面阻挡,从而提高其进入胰腺的概率。研究团队将该机制命名为“包膜过滤介导的胰腺靶向”(CAMP)。
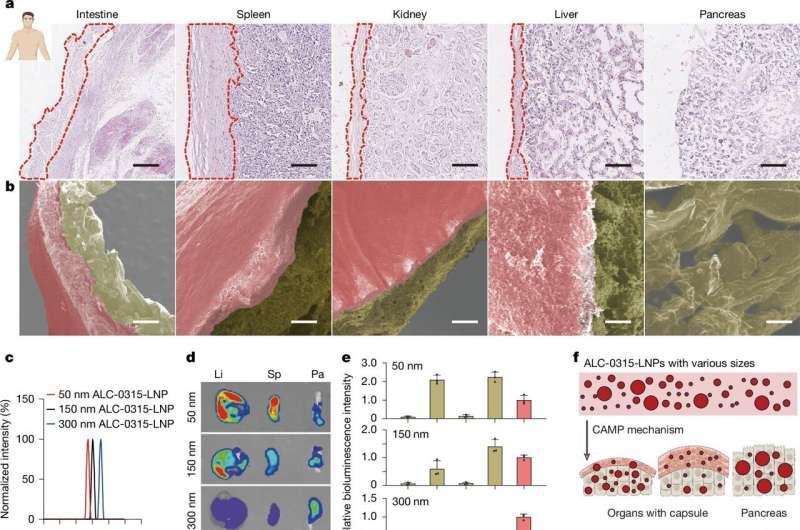
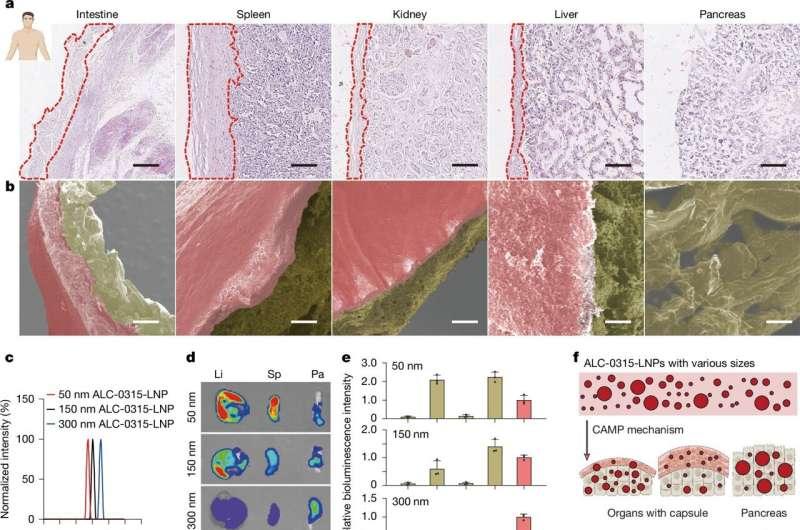
在小鼠实验中,研究人员比较了不同尺寸LNPs的体内分布:较小颗粒仍主要聚集于肝脏和脾脏;中等尺寸颗粒以肝脏为主要靶向;而约300纳米的较大颗粒会被肝脏和脾脏的包膜阻挡,但能够进入包膜相对“薄弱”的胰腺。
体内“增大”的可扩展纳米颗粒
研究团队同时指出,单纯增大颗粒尺寸会带来新的递送难题:颗粒过大可能不利于细胞摄取。为此,团队设计了一种“可扩展”纳米颗粒,其初始尺寸约为100纳米,在腹腔注射后与局部蛋白质相互作用并迅速增大至300纳米以上。研究人员称,在增大后,该颗粒可被肝脏和脾脏包膜过滤,从而更易到达胰腺;到达胰腺后,颗粒可进入胰腺细胞并递送mRNA指令。
研究团队在论文中写道,他们揭示了器官包膜作为过滤器的作用,可阻止腹腔内注射的大尺寸纳米颗粒进入多数腹部器官,从而实现胰腺靶向递送。
药物测试结果与下一步计划
研究人员在动物模型中测试了两类递送内容。其一为CRISPR-Cas9相关指令,用于沉默导致免疫系统攻击胰腺的基因;研究称,单次治疗后,小鼠自身免疫破坏被阻断超过180天。其二为递送IL-2(白细胞介素-2),用于增强机体自然防御;研究称,在与癌症疫苗或CAR T细胞疗法联合使用时,该治疗使部分肿瘤缩小并清除其他肿瘤。
研究团队表示,在非人灵长类动物完成安全性测试后,他们认为该技术已具备进入人体试验阶段的条件。围绕该研究的新闻与观点文章亦发表于《自然》杂志。











