康奈尔大学研究团队近日披露一项关于细胞应激调控的新发现:蛋白质SHKBP1与关键蛋白p62之间的相互作用,可能帮助细胞维持重要“回收系统”的平衡,使细胞在压力条件下作出适度反应。研究人员指出,这一平衡在癌症及神经退行性疾病等情形中可能出现失调。
相关论文于2月6日发表在《细胞生物学杂志》(Journal of Cell Biology)。研究由康奈尔大学生物化学、分子与细胞生物学系博士生林峦,以及化学与化学生物学系生命科学Nancy和Peter Meinig家族研究员、韦尔细胞与分子生物学研究所副教授Jeremy Baskin共同领导。
Baskin表示,细胞持续面临来自正常代谢或环境损伤的多种压力。蛋白质p62在细胞回收机制中处于核心位置,其作用之一是将受损蛋白质聚集到被称为“p62体”的区室中,以便后续处理。
研究同时强调,p62的活性需要保持在适当水平:活性过低可能导致有毒蛋白质积累,这在阿尔茨海默病和帕金森病中有所体现;活性过高则可能使系统过度活跃,在多种癌症中,癌细胞会利用回收过程的产物促进肿瘤生长。
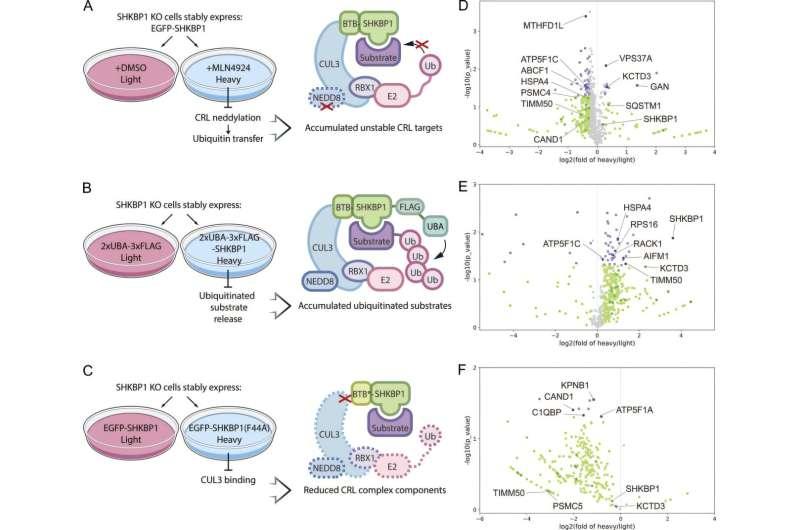
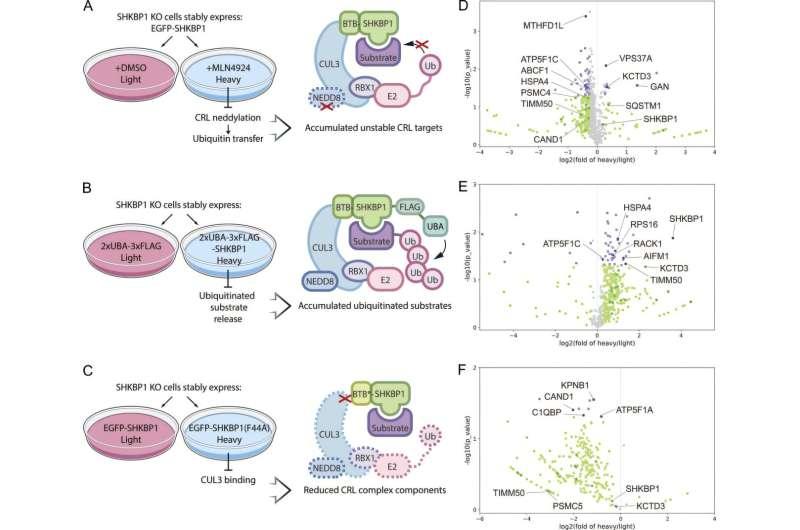
为在活细胞内观察两种蛋白的相互作用,团队结合了生化与成像等技术。研究人员发现,SHKBP1可直接结合p62的一段结构区域,而该区域通常允许p62聚集成较大的簇。Baskin称,这种结合在物理层面阻止了p62分子进一步聚集成大型结构。实验显示,去除SHKBP1会使p62体变得更大且流动性降低;增加额外的SHKBP1则会使p62体更小并更具动态性。
研究还将这一机制与细胞抗氧化防御系统Keap1–Nrf2通路联系起来。该通路在正常条件下维持平衡,在细胞遭受压力时启动保护反应以限制损伤。p62在其中发挥作用,通过帮助去除抑制抗氧化反应的蛋白质。新研究认为,SHKBP1通过调控p62的行为,间接影响Keap1–Nrf2通路,从而参与决定保护反应的激活强度。
研究人员指出,癌细胞常劫持该通路以抵抗化疗;而在神经退行性疾病中,神经元则可能在最需要时未能有效激活该通路。
Baskin表示,尽管该研究聚焦基础细胞机制,但其与人类疾病之间存在潜在关联。其团队认为,进一步理解SHKBP1如何影响上述平衡,未来或可为治疗策略提供新的思路。例如,若SHKBP1功能丧失会自然增强Nrf2反应,或可探索在大脑中安全抑制SHKBP1以实现神经保护的可能性。












