抗生素抗性(AR)近年来持续加速,被视为全球健康危机之一。随着致病细菌不断演化出逃避多种药物治疗的机制,“超级细菌”数量增加。有研究预计,到2050年全球每年相关死亡人数可能超过1000万。
为应对这一紧迫威胁,科研人员正探索新技术手段,尤其针对在医院环境、污水处理区域、畜牧场及鱼类养殖场等场景中更易繁盛的抗生素抗性细菌。加州大学圣地亚哥分校(UC San Diego)研究团队近日公布一项基于CRISPR的遗传学工具,旨在从细菌群体中去除或禁用抗生素抗性元素。
据介绍,该校生物科学学院Ethan Bier教授与Justin Meyer教授团队合作,开发了一种名为pPro-MobV的第二代“主动遗传学”(Pro-Active Genetics,Pro-AG)工具。研究人员将其描述为借鉴“基因驱动”思路的群体工程方法:通过让少量携带特定遗传组件的细菌在群体中扩散关键失活元素,从而在更大范围内中和目标群体的抗生素抗性。
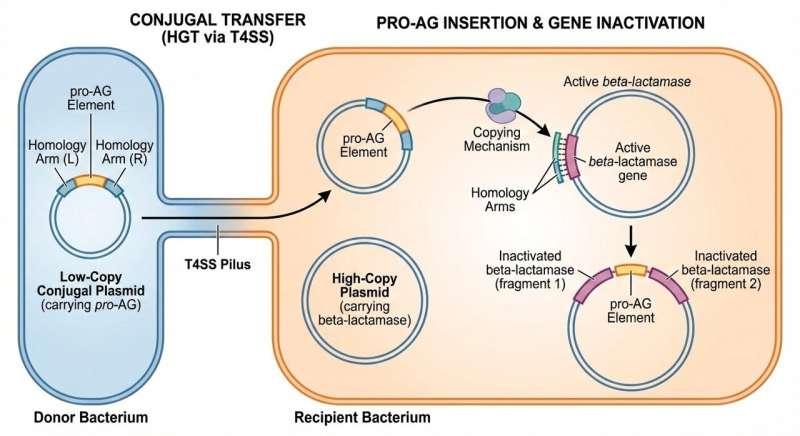
Bier表示,pPro-MobV将基因驱动理念从昆虫研究拓展至细菌体系,并作为一种群体层面的工程工具使用;借助CRISPR技术,可从少数细胞出发,逐步在大规模目标群体中实现对抗生素抗性成分的中和。
研究团队回顾称,2019年Bier实验室曾与该校医学院Victor Nizet教授团队合作提出最初的Pro-AG概念:将一个“遗传盒”导入并在细菌基因组间复制,使抗生素抗性成分失活。该遗传盒会自我插入携带在质粒上的抗生素抗性基因中。质粒为细胞内可复制的环状DNA,研究人员称该过程可使细菌恢复对抗生素治疗的敏感性。
在上述工作基础上,研究人员进一步开发了可通过接合转移传播的后续系统,使抗生素CRISPR遗传盒组件能够在细菌之间扩散。研究团队在《自然》旗下期刊《npj Antimicrobials and Resistance》发表的论文中称,pPro-MobV系统可利用细菌细胞间自然形成的“交配通道”传递关键失活元素,并在细菌生物膜中验证了该过程的有效性。
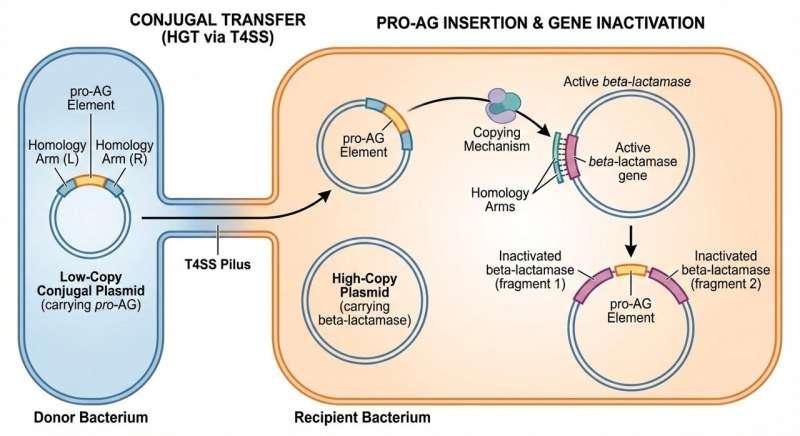
研究人员指出,生物膜是由微生物构成的群落,可污染多种表面,且在常规清洁方式下难以去除。生物膜还与疾病传播相关,并被认为是多种严重感染形成的重要因素之一,因为其形成的保护层会降低抗生素渗透,从而帮助细菌抵抗药物。研究团队认为,该技术在医疗环境、环境修复以及微生物组工程等方向具有潜在应用价值。
Bier表示,在抗击抗生素抗性过程中,生物膜环境尤为关键,因为在临床或封闭环境(如水产养殖池塘、污水处理厂)中,生物膜是最具挑战性的细菌生长形态之一。他同时提到,若能减少抗性从动物向人类的传播,可能对整体抗生素抗性问题产生重要影响,并称有估计认为约一半的抗性来自环境。
此外,研究人员还报告称,主动遗传系统的组件可由噬菌体携带并传递。噬菌体是细菌的病毒性“竞争对手”,目前也被用于设计对抗抗生素抗性的方法,例如通过规避细菌防御并将破坏性因子导入细胞。研究团队设想,pPro-MobV元素可与此类工程化噬菌体协同使用。该平台还可整合一种高效的同源性删除过程,作为安全措施,在需要时移除遗传盒。
Meyer表示,据其所知,这项技术属于少数能够主动逆转抗生素抗性基因传播的方法之一,而不仅是减缓或被动应对其扩散。











