身体结构的形成并非依赖预先写定的“蓝图”,而是在胚胎发育过程中由基因网络的精密激活与抑制共同驱动。日本理化学研究所(理研)研究人员近日在重建脊椎动物胚胎关键构建模块——体节——的形成机制方面取得进展。
体节是在发育早期由部分细胞形成的平行结构带,最终发育为脊柱、肋骨和肌肉。体节的生成与一组基因的周期性活动有关,这一机制通常被称为“分节时钟”,其中多种相关基因已被识别。
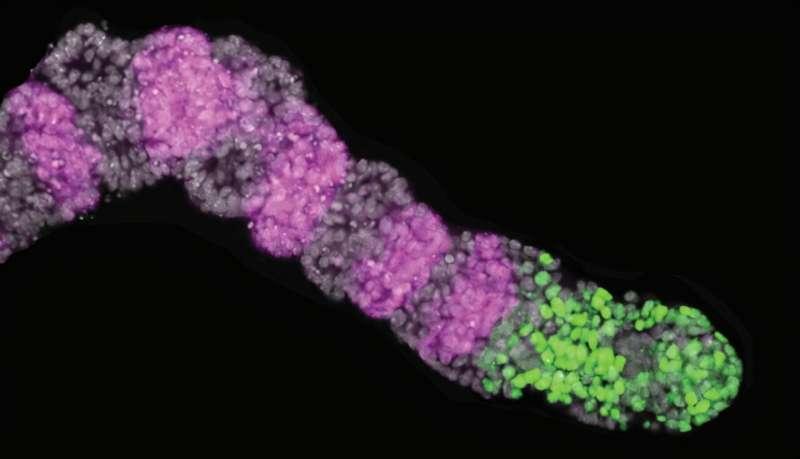
理研生物系统动力学研究中心的影山良一郎表示,尽管分节时钟的存在已为人所知,但“产生同步振荡并像波浪一样传播于胚胎组织中的分子步骤尚未完全明了”。由于相关基因活动在胚胎内变化迅速,分节时钟在体内的可视化与操控长期面临技术难题。
为解决这一问题,影山及其同事采用新近开发的技术工具,通过基因工程将小鼠干细胞诱导分化为“诱导前体体节中胚层”(induced presomitic mesoderm,iPSM)。研究团队称,该组织可高度模拟通常产生体节的胚胎前体组织。相关成果分别发表于《Development》和《Genes & Development》两篇论文。
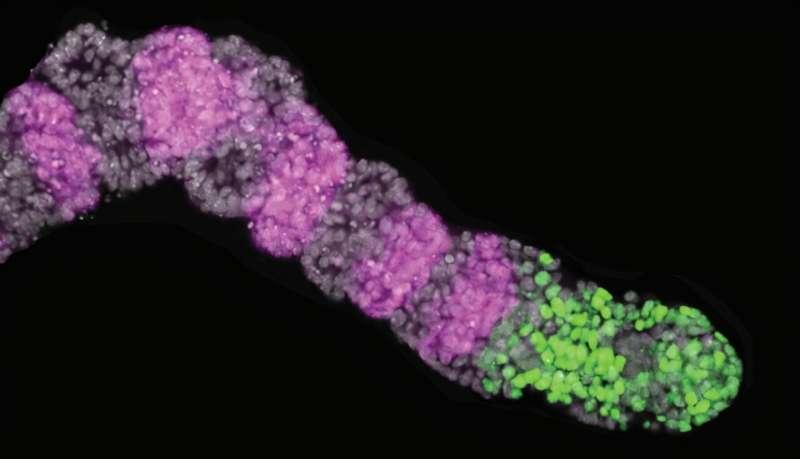
影山表示,这些iPSM模型保留了体内分节时钟的关键特征,使团队得以进一步描述关键振荡基因Hes7在体节形成中的作用。研究显示,Hes7可抑制信号通路中下游基因的表达。团队在筛选靶标时关注到Cdh2:该基因编码一种细胞黏附蛋白,通常作为“分子胶水”将细胞黏合在一起,从而影响胚胎组织的模式形成与分节过程。
研究人员通过在iPSM构建体中操控基因表达,并结合活细胞显微镜观察效应,发现Hes7对Cdh2的调控会直接影响成纤维生长因子(FGF)信号通路。该通路为体节分节过程中细胞成熟的时序提供发育指令。研究还指出,当Hes7表达异常导致Cdh2活性异常时,细胞间黏附会出现不规则,从而破坏发育中体节的结构完整性。
影山表示,这一结果为振荡基因表达与信号通路之间提供了新的分子连接线索,揭示时间信息如何在胚胎发生过程中转化为空间模式。他认为,这项工作是团队实现对体节形成过程进行全面时空重建的重要一步。











