东京科学研究人员在一项研究中披露,先天免疫识别病毒RNA的早期环节中,遗传学与生理学实验室2(LGP2)与黑色素瘤分化相关蛋白5(MDA5)可通过协同作用提升对短双链核糖核酸(dsRNA)的响应效率。研究团队结合冷冻电子显微镜与高速原子力显微镜等技术,观察到LGP2与病毒RNA结合并招募MDA5分子,形成类似“串珠”的装配过程,从而为后续信号复合体的形成提供支架,触发先天免疫反应。
先天免疫对病毒dsRNA的识别
研究指出,先天免疫系统是机体抵御病毒感染的第一道防线。病毒进入细胞后,复制过程中通常会产生dsRNA。细胞质中的免疫受体持续搜索dsRNA作为感染标志。其中,MDA5通过识别病毒dsRNA并沿其组装成丝状结构发挥关键作用;当足够数量的MDA5分子完成组装后,可引发信号级联反应,最终促使细胞产生抗病毒物质。
除MDA5外,LGP2同样参与病毒RNA的检测。LGP2能够结合病毒RNA,并通过依赖能量的转位过程沿RNA移动。尽管LGP2本身不直接传递抗病毒信号,但此前研究已提示其与MDA5协同参与病毒感染的识别;不过,LGP2如何识别病毒RNA并促进MDA5发挥作用的具体机制仍不明确。
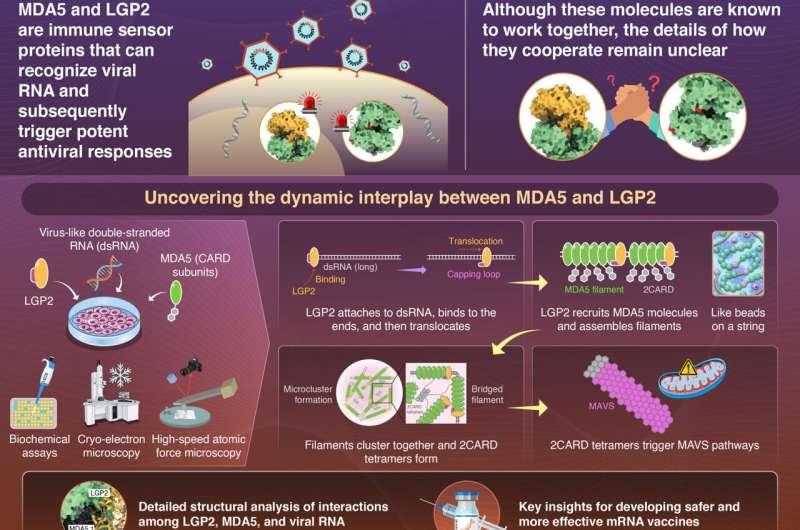
冷冻电镜与高速原子力显微镜捕捉协作过程
为厘清上述机制,日本东京科学综合研究所机制免疫学研究组助理教授(终身教职)加藤一树领导团队,与东京大学理学院生物科学系沼木治教授及研究生栗原仁奈(研究期间)合作,结合生化实验与成像手段,系统分析LGP2与MDA5的相互作用及其与病毒RNA的结合方式。相关成果于2026年2月19日发表在《分子细胞》(Molecular Cell)。
研究人员首先发现,LGP2在病毒RNA分子较短时作用更为突出。实验显示,MDA5单独更倾向于对长链dsRNA产生响应;而在LGP2存在的情况下,MDA5即便面对较短RNA分子,也能有效形成短丝状结构并激活下游抗病毒信号。
在结构与动态观察中,团队利用冷冻电子显微镜解析蛋白结构,并通过高速原子力显微镜追踪装配过程。结果显示,LGP2会优先结合在dsRNA分子的末端,随后借助ATP提供的能量沿RNA链移动。在这一过程中,LGP2充当“支架”,在其后方招募MDA5分子并促进其组装为稳定的丝状结构。研究人员将该过程比喻为“串珠”:RNA链如同线,LGP2则类似引导后续MDA5“珠子”排列的起始节点。
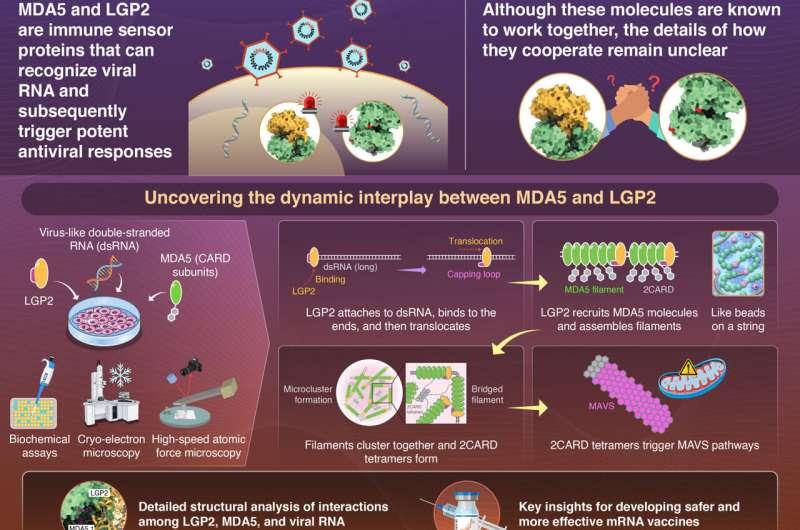
促进MAVS激活并放大抗病毒信号
研究还显示,LGP2可促进MDA5丝状结构形成小簇,这些簇进一步增强线粒体抗病毒信号蛋白(MAVS)的激活。MAVS被认为是细胞内放大抗病毒反应的关键蛋白。加藤一树表示,研究阐明了LGP2识别病毒RNA并与MDA5协作激活免疫反应的精确机制。
研究团队认为,该发现为抗病毒防御的关键早期步骤提供了更清晰的分子层面图景,并可能为未来在抗病毒疗法及基于RNA的医疗技术中更精细地调控免疫反应提供参考。加藤一树称,这些结果加深了对病毒RNA识别过程的理解,预计将有助于设计更安全、更有效的mRNA疫苗。











