一支合作研究团队报告称,来源于日本屋久岛附近海域深海海绵的结构复杂肽类天然产物yaku'amide B,存在此前未被明确的作用机制。研究人员表示,天然产物因结构复杂,往往通过与多种生物分子发生短暂相互作用而呈现多面生物活性。此前研究已证实yaku'amide B可抑制细胞能量生产所必需的ATP合酶,但该机制不足以完全解释其独特的抗癌特性。
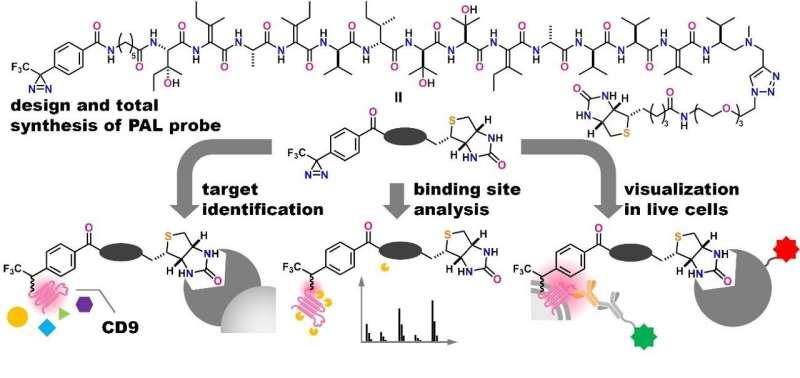
为进一步厘清其作用方式,东京农业技术大学樱井香教授团队与东京大学药学院伊藤浩明副教授、井上正之教授合作,采用光亲和标记(PAL)技术开展研究。该技术可用于“捕获”与药物发生短暂相互作用的分子,从而识别潜在靶点。
研究成果发表于《美国化学会杂志》。
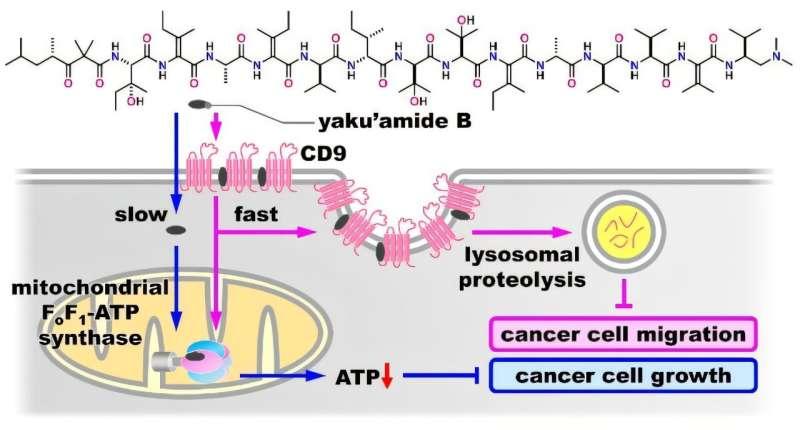
伊藤浩明在介绍结果时称,研究团队通过设计的PAL探针发现,yaku'amide B会短暂结合CD9——一种被报道为癌症干细胞标志的膜蛋白。研究同时观察到,这种相互作用会促进癌细胞内CD9的降解。与此同时,yaku'amide B还能进入线粒体并抑制ATP合酶,导致细胞能量耗竭。
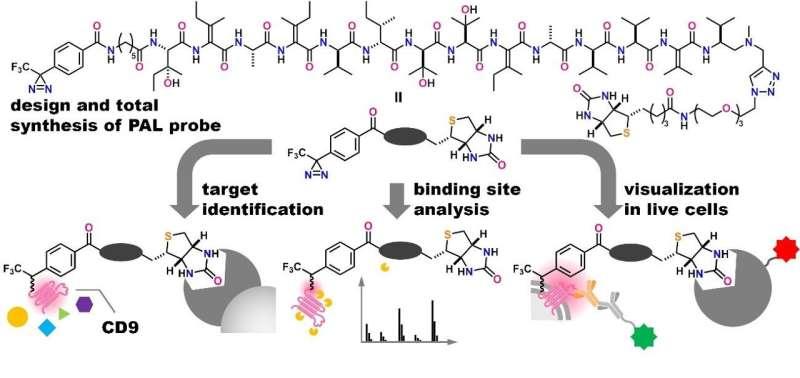
樱井香表示,CD9被视为包括复发和转移相关的侵袭性癌细胞的关键标志,yaku'amide B能够诱导CD9降解的发现具有开创性意义,并为靶向癌症干细胞及其相关通路的药物开发策略提供了新的可能。
井上正之指出,ATP耗竭与CD9降解的双重机制,为yaku'amide B抑制癌细胞增殖与迁移的能力提供了更有力的解释。研究团队称,yaku'amide B是首个被报道可诱导CD9降解的天然产物,同时也凸显PAL在研究短暂相互作用方面的应用价值。
研究人员表示,该工作进一步显示天然产物可作为创新治疗方法的起点,并涉及多靶点药物设计与蛋白降解策略等方向。
发表评论
登录后才可评论。
去登录











