东京科学研究人员报告称,免疫球蛋白G(IgG)中长期较少受到关注的下铰链区域,可能在维持抗体结构稳定性与免疫功能方面发挥关键作用。研究显示,在该区域删除单个氨基酸残基,即可使全长IgG1抗体转变为稳定的半尺寸IgG1分子,并伴随免疫活性改变。
上述研究发表于《药物化学杂志》(Journal of Medicinal Chemistry)。研究由日本东京科学研究所(Science Tokyo)副教授柳中冴子与研究生古关悠希牵头,并与九州大学、名古屋大学及日本自然科学研究所研究人员合作完成。
研究团队指出,IgG抗体通常呈Y形结构,在循环抗体中占比约75%。其主要由两部分功能单元构成:负责识别抗原的Fab区域与向免疫系统传递信号的Fc区域,两者通过铰链片段连接并协同工作。
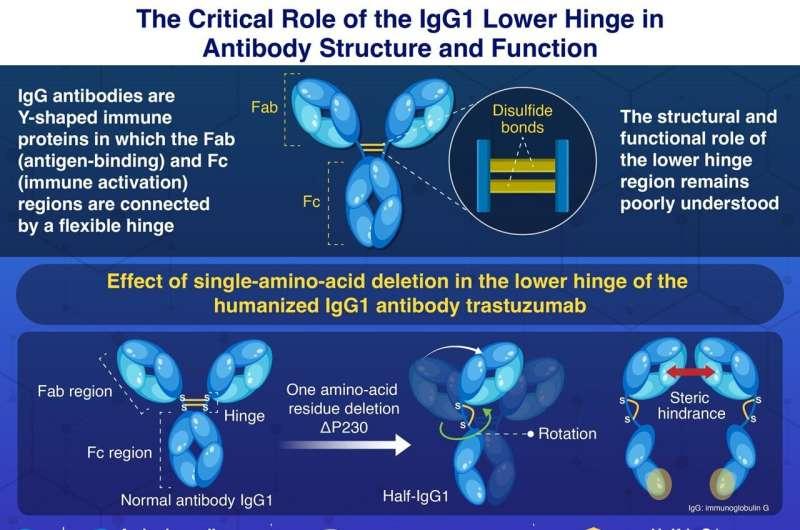
研究人员表示,为评估下铰链在塑造IgG1结构与功能中的作用,他们对下铰链区域残基进行了系统性删除实验。团队以在癌症治疗中靶向HER2蛋白的人源化IgG1抗体曲妥珠单抗为模型,在其铰链区域开展氨基酸替换与缺失研究。
结果显示,删除单个脯氨酸残基(Pro230)后,抗体出现约75千道尔顿的半尺寸产物,即半IgG1分子。研究称,在这一构型中,原有二硫键连接模式受到破坏,两条重链不再保持稳定连接。
成像研究进一步显示,半IgG1分子中Fab与Fc区域的相对取向发生变化。研究人员描述称,在正常IgG抗体中,Fc区域的排列有利于两半配对并与免疫受体相互作用;而在半抗体中,该配对界面发生向内旋转并朝向Fab区域,可能造成Fab臂的物理干扰,从而阻碍Fc区域形成正常二聚体。
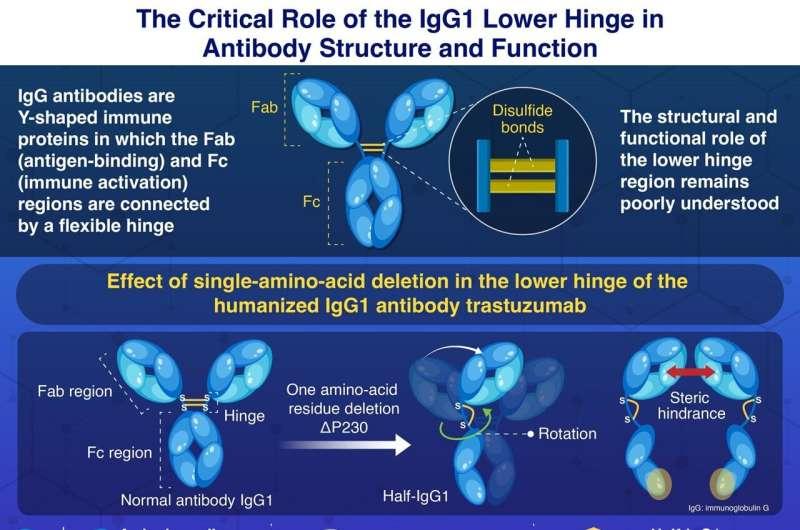
研究同时指出,尽管结构发生改变,半抗体并未完全失去功能。其仍可通过单一界面与高亲和力免疫受体FcγRI结合,并触发免疫信号,但效率低于全长抗体。
研究团队据此认为,下铰链在维持IgG1形状、稳定性与功能方面具有决定性作用,并将其描述为IgG1的结构与功能“控制枢纽”。研究人员表示,这一发现为设计免疫效应可精确定制的治疗性抗体提供了思路,潜在适用方向包括癌症与自身免疫疾病等领域。











