在《细胞外囊泡杂志》发表的一项研究中,佛罗里达大学健康癌症研究所的研究人员提出一种基于细胞外囊泡(extracellular vesicles,EVs)的药物递送策略,旨在提升针对三阴性乳腺癌的靶向治疗效果。研究团队表示,该递送系统有望同时缓解靶向药物在肿瘤部位“难以到达”以及在体内“运输不稳定”的两项常见问题。
佛罗里达大学药学院药剂学系博士生Nina Erwin在研究中表示,团队的核心问题是评估细胞外囊泡能否克服靶向药物递送效率不足与稳定性欠佳的限制。
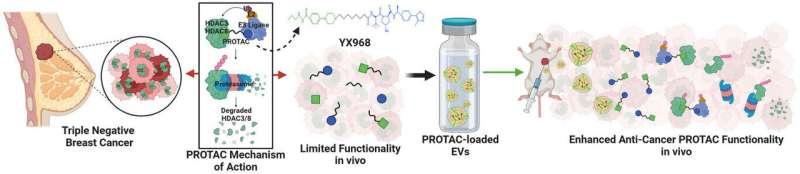
研究显示,当细胞外囊泡装载蛋白酶体靶向嵌合体(PROTACs)后,在小鼠模型中观察到肿瘤生长显著减缓,且存活率提高。研究人员介绍,PROTACs通过诱导细胞内蛋白酶体降解过程清除异常蛋白质,从而阻断肿瘤形成相关机制。
研究团队指出,提高细胞外囊泡对PROTACs的递送效率,可能对三阴性乳腺癌治疗具有重要意义。该类型肿瘤分子组成多样、对不同疗法敏感性存在差异,并具有生长快、侵袭性强、早期转移及复发率高等特点。

研究人员同时提到,尽管PROTACs在体外实验中显示潜力,但在活体系统中的疗效受到多重因素限制,包括肿瘤穿透能力有限,以及药物在到达肿瘤部位过程中易分解等。
为应对上述障碍,团队引入细胞外囊泡作为“载体”,将一种特定类型的PROTACs装载其中。研究人员称,该药物旨在抑制乳腺癌肿瘤生长,同时避免引发健康细胞功能障碍。

Erwin表示,这一方法不仅提升了药物与载体的结合效率,也增强了药物在运输过程中的稳定性,从而更有利于药物到达肿瘤部位并发挥作用。她还称,这项概念验证研究为将细胞外囊泡作为递送平台的应用提供了可能性,潜在适用范围不局限于单一药物或单一癌种,并可能推动PROTACs等药物向临床应用迈进。
论文资深作者、药剂学系副教授Mei He表示,解决递送难题可能加速其他类似药物的临床转化。她还提到,该研究来自跨学科合作,并感谢医学院及佛罗里达大学药物化学系同事的贡献与支持,这些合作补充了其团队在细胞外囊泡及相关工程领域的研究基础。











