近三十年前,科研人员在动物癌症模型中观察到,黑麦花粉中的一对分子可在未知且无毒的机制下减缓肿瘤生长并帮助清除肿瘤。然而,由于缺乏对分子精确结构的确认,相关研究长期停滞。
西北大学化学家近日通过从零开始的全合成策略,确定了这两种分子——黑麦苷A和黑麦苷B——的三维结构,为后续解析其活性来源及作用方式提供了关键“蓝图”。相关成果已发表在《美国化学会杂志》上。
论文通讯作者、西北大学韦恩伯格文理学院化学教授卡尔·A·谢德特表示,早期研究提示黑麦花粉可能通过一种尚不清楚且无毒的机制在多种动物模型中发挥抗肿瘤作用;在结构被确认后,研究团队将能够进一步定位分子中发挥作用的部分,并据此探索制造更优版本的可能性。
研究团队指出,天然产物长期以来为药物研发提供线索。谢德特在研究中提到,天然产物未必可直接成为有效药物,但可作为先导化合物,为通过化学手段改造以提升口服可用性、代谢稳定性及靶向性提供基础。
在黑麦花粉相关应用方面,全球已有消费者以补充剂形式摄入黑麦花粉提取物以维护前列腺健康,但其尚未被优化为药用药物。研究人员认为,要理解其潜在作用机制,需要掌握分子的精确三维形状,而这一信息此前一直难以获得。
据介绍,传统结构解析手段(如先进核磁共振光谱)未能完全厘清分子关键部位的空间取向,导致关于黑麦苷A和B存在两个竞争性结构模型。两种模型在原子组成、连接方式与整体形状上相同,但分子核心部分互为镜像;这一差异可能影响分子与生物靶点的结合方式,并决定其是否具有生物活性。
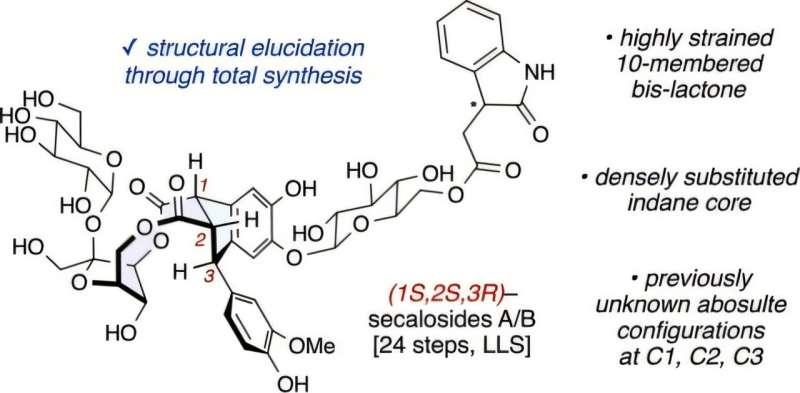
为解决争议,团队采用全合成路线在实验室逐步构建天然分子。研究称,黑麦苷A和B的核心包含一个罕见且高度受力的紧密10元环结构,合成难度较高。团队先构建更大且更灵活的环,再通过触发反应使其在一步内转化为更小、受力更强的环结构。随后,研究人员分别合成两种竞争结构版本,并与从黑麦花粉中分离的样品进行比对,最终确认仅有一个版本与天然样品完全一致,从而锁定真实结构。
谢德特表示,团队已证明能够合成该天然产物的核心结构,下一步将寻求与免疫学领域的潜在合作伙伴,以推进与临床应用相关的研究工作。











