研究人员表示,基因调控机制可能比此前认为的更具可预测性。相关团队在《自然》杂志发表论文,介绍其开发的深度学习模型PARM,并称该模型有望帮助解释基因在何时、何地以及以何种强度被开启或关闭的调控规则。
论文共同通讯作者、荷兰癌症研究所(NKI)及Oncode研究所小组负责人Bas van Steensel指出,经典遗传密码解释了DNA中的基因如何编码蛋白质,但对多数基因而言,科学界仍难以理解其调控方式。研究人员已知基因之间的DNA包含启动子等调控元件,但决定基因是否开启或关闭、在哪类细胞中发挥作用以及表达强度的“控制系统语言”长期缺乏清晰描述。

研究团队称,这一问题与癌症研究密切相关,因为多数与癌症相关的突变位于基因组的非编码区域,而对这类突变的解释一直较为困难。团队表示,PARM模型为评估此类调控突变的功能影响提供了新的工具。
PARM模型在Oncode研究所发起的PERICODE项目框架下开发。该项目联合七个研究团队协作推进。研究人员介绍,van Steensel所在实验室开发的一项技术,使得基因调控测量能够以前所未有的规模开展:通过数百万次精心控制的测量,捕捉短DNA序列如何影响基因活性。
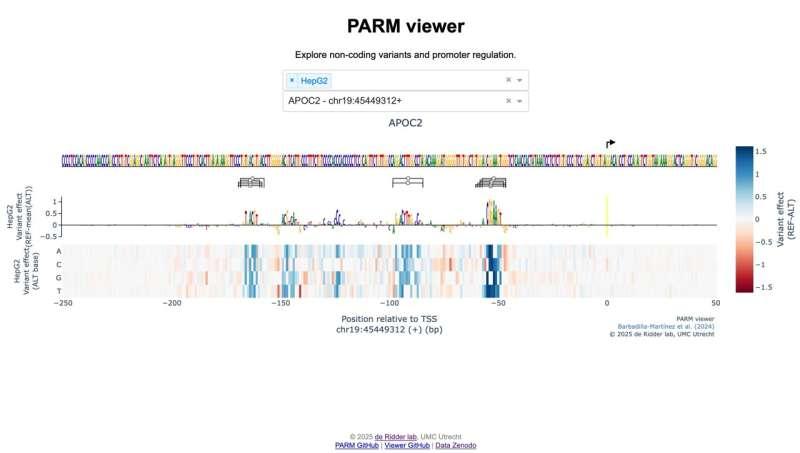
在此基础上,乌得勒支大学医学中心(UMC Utrecht)及Oncode研究所的Jeroen de Ridder研究组负责将大规模实验数据用于训练人工智能模型。de Ridder表示,与多数从既有数据中学习的AI模型不同,该研究中“测量与AI共同设计”,从而能够为特定细胞类型构建高效模型,并将应用规模扩展到此前难以想象的程度。
研究团队称,新模型可用于预测不同细胞类型之间的基因调控差异,以及细胞在药物等刺激条件下的调控变化;同时,模型还能以较高细节刻画每个基因“开关按钮”的结构。研究人员强调,团队并未止步于计算预测,模型输出均经过严格实验验证,以确保预测结果的准确性。

van Steensel表示,PARM使研究人员能够在更大规模上揭示调控规则,从而理解并预测调控DNA如何控制基因活性。研究团队同时指出,现有AI模型要么体量过大、难以用于海量突变的评估,要么过于通用、难以充分捕捉细胞类型差异;PARM旨在改善这一局面,使研究人员能够在特定细胞类型及特定条件(如药物处理)下预测调控突变的功能影响,并为癌症诊断、患者分层及未来疗法提供线索。

论文还提及,谷歌DeepMind近期在《自然》发表了旨在理解基因调控的模型AlphaGenome。van Steensel称其为“很棒的模型”,并表示PARM在实验与计算上更为轻量,所需计算能力约为AlphaGenome的千分之一,从而更便于全球学术研究者使用。他补充称,借助该模型,研究人员可在较短时间内观察特定细胞类型(如肿瘤细胞)如何利用DNA编码来响应激素、营养或药物等信号。
PERICODE项目参与团队包括:Bas van Steensel(NKI)、Jeroen de Ridder(UMCU)、Emile Voest(NKI)、Michiel Vermeulen(NKI)、Lude Franke(UMCG)、Sarah Derks(阿姆斯特丹UMC)、Wilbert Zwart(NKI)。











