经过十余年研究,科研人员报告称已厘清一种被称为“铁死亡”的细胞死亡形式在生理条件下的自然触发机制。相关论文发表于《Cell》最新一期,研究团队表示,该发现为探索癌症及神经退行性疾病等领域的潜在治疗策略提供了新的分子线索。
铁死亡临床转化长期受限
铁死亡是一种依赖铁的细胞死亡方式,其机制不同于更为常见的细胞凋亡、坏死等路径。尽管铁死亡长期被视为可能的肿瘤抑制手段,但将其转化为临床应用一直面临障碍。
论文通讯作者、赫伯特·欧文综合癌症中心癌症基因组与表观基因组项目成员魏谷表示,过去相关实验多依赖化学方式诱导铁死亡,“问题在于几乎所有实验都需要化学诱导”。研究指出,实验室常用的化学诱导物质本身并不适合作为药物;同时,化学诱导路径涉及的蛋白GPX4失活对动物致死,提示若以该路径为靶点可能带来毒性风险,从而使研究与应用推进受阻。
从p53线索出发寻找天然信号
研究团队回溯铁死亡的天然调控线索。魏谷团队在2015年曾发现,天然肿瘤抑制基因p53是铁死亡诱导路径的关键组成部分,但当时尚不清楚该过程还涉及哪些分子。魏谷称,当年论文提出“必须识别天然信号”,而在随后十年的工作中,团队最终找到了相关路径。
团队表示,研究周期较长的原因之一在于缺乏明确线索:既有文献主要聚焦经典的化学诱导路径,难以直接指向生理条件下的触发机制。为此,研究人员与哥伦比亚大学及其他机构的合作者开展了更广泛的筛查工作。
CRISPR筛选锁定GPX1相关通路
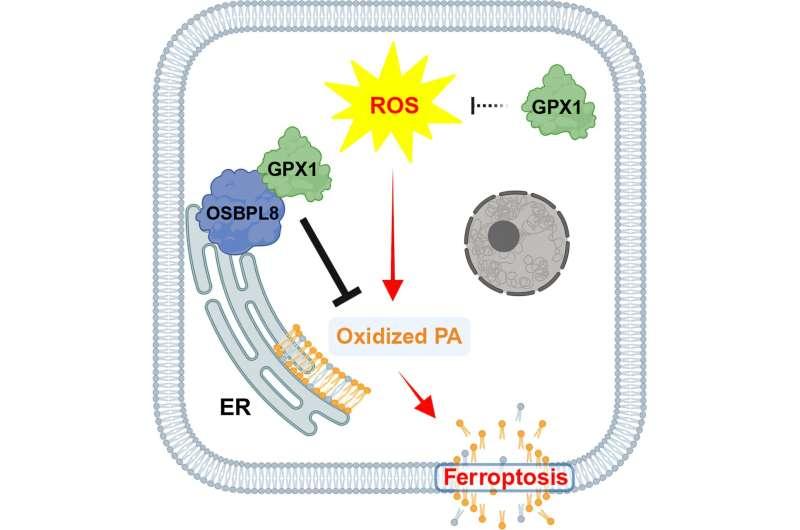
研究人员使用CRISPR-Cas9基因编辑系统,对培养的癌细胞基因组进行逐一敲除筛选,寻找那些失去对活性氧(ROS)诱导铁死亡能力的细胞。筛选结果显示,GPX1基因是天然诱导铁死亡的关键组成部分。研究团队随后以GPX1为起点,进一步识别出该天然铁死亡通路的其他构成要素。
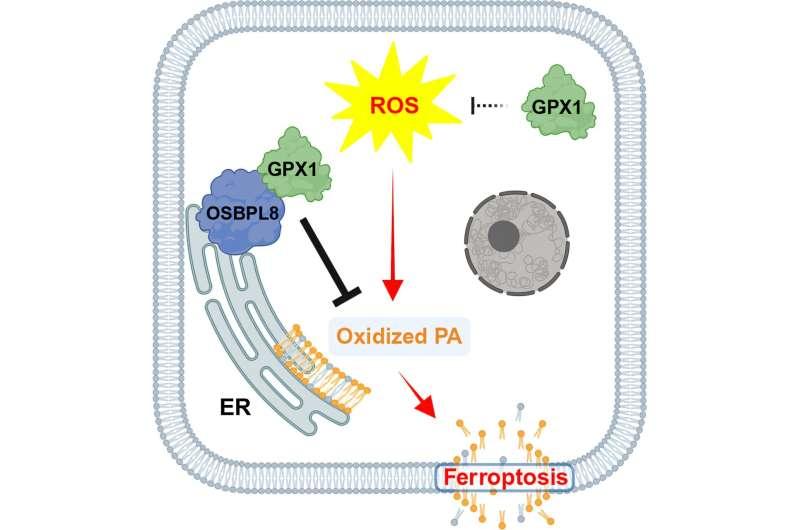
论文描述,这是一套协同运作的蛋白质与脂质系统,可感知并响应细胞内高水平ROS。研究人员指出,ROS等活性分子会持续损害细胞系统,细胞需要降低损伤;在极端情况下,细胞会通过自我清除避免危及机体,而铁死亡即为实现这一过程的机制之一。研究同时提到,癌细胞通常会抑制此类路径,而此次工作为“按需诱导铁死亡”提供了新的研究方向。
研究认为GPX1具备潜在靶点特征
研究对比了GPX4与GPX1在细胞生存中的作用差异:GPX4对细胞生存至关重要,而GPX1在一般情况下并非必需,只有当细胞内ROS水平极高时才变得关键。研究还称,GPX1基因失活的动物可正常发育,为进一步研究铁死亡提供了模型系统,并提示针对GPX1的干预可能具有不同于GPX4路径的安全性特征。
魏谷表示,癌细胞增殖速度快,产生的ROS水平显著高于正常细胞,“正常组织能耐受GPX1的缺失,但癌细胞绝对依赖GPX1生存”。研究同时提到,高ROS水平也是亨廷顿病、帕金森病等神经退行性疾病的特征之一。
论文第一作者、魏谷实验室博士后研究员夏章川表示,团队对以GPX1为靶点开发癌症及其他疾病新疗法的潜力感到兴奋。魏谷补充称,团队已着手开发GPX1抑制剂,并表示其设想是尽量不影响正常细胞、主要作用于癌细胞或其他病理细胞,从而有望降低副作用。












