聚合物胶束是一类由同时含亲水段与疏水段的聚合物链在溶液中自组装形成的纳米级颗粒,可用于包裹难溶药物,因而被视为药物输送与纳米医学的重要载体之一。
在多种胶束形成材料中,Poloxamer 407(P407)因其温度响应特性受到关注:随温度升高可由液态转变为软凝胶,并在接近体温时表现出较高稳定性。相关温度依赖的凝胶行为被认为有助于实现药物缓释,从而降低给药频率并减少副作用。
不过,研究人员指出,P407的溶胶—凝胶转变难以仅用单个胶束的行为解释,其关键在于胶束之间的相互作用及其排列方式。现有认识多来自纯水体系实验,而人体内液体环境更为复杂;同时,一些理论模型依赖对聚合物胶束并不适用的假设,使得在模拟体液的盐水溶液中,胶束间作用力的特征仍不清晰、也难以预测。
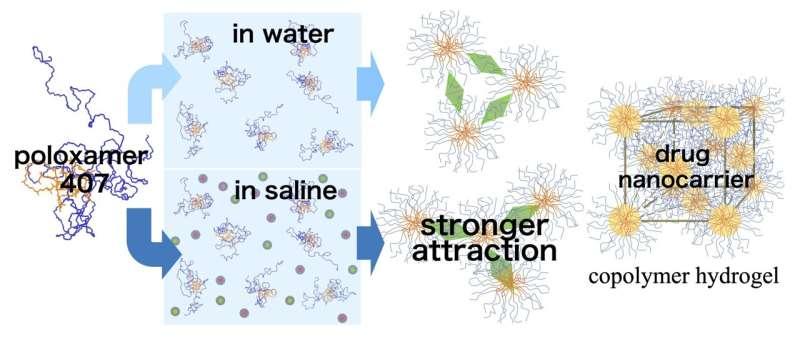
为弥补这一空白,日本千叶大学理学院副教授森田毅带领团队对盐水环境中的P407胶束相互作用开展实验研究。论文发表于《胶体与界面科学杂志》(Journal of Colloid and Interface Science),合著者包括千叶大学的高松俊介、东健次郎、斋藤美波,日本长滨生物科学技术研究所的今村浩,以及日本室兰工业大学的角友成。
研究团队以溶解于磷酸盐缓冲盐水(PBS)的P407胶束为对象,在不预设胶束行为模式的前提下,基于实验数据对接近体内环境条件下的相互作用进行量化,并结合两种互补表征手段:其一,小角X射线散射用于探测胶束在纳米尺度上的相对位置与集体结构;其二,动态光散射通过追踪散射光波动,测量单个聚合物链、胶束及更大聚集体的尺寸与运动特征。
综合两类数据后,研究人员计算了“对间相互作用势”,以定量描述两个胶束随距离变化的吸引或排斥强度。结果显示,随着温度升高并接近凝胶形成,胶束间距趋于更规律,彼此略微远离但仍保持连接。研究团队将这一行为与熵驱动的阿尔德转变(Alder transition)相联系,即粒子通过更有序的排列获得更大的热运动自由度。
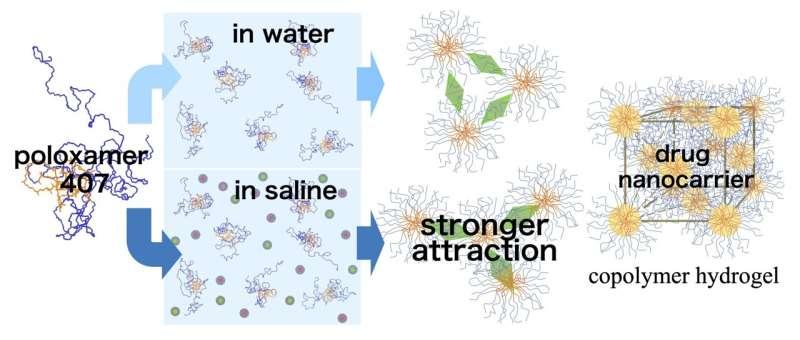
研究同时发现,在PBS中胶束间吸引力较纯水更强,使胶束结合更紧密,限制了其分离距离,进而导致凝胶结构波动增加、排列均匀性下降。团队进一步指出,这些差异会影响凝胶稳定性:盐水中形成的凝胶在较低温度下出现破裂,提示随温度升高而增强的结构波动会削弱凝胶并使其更早崩溃。
森田毅表示,通过加深对控制药物纳米载体性质的胶束间相互作用的理解,有望阐明并预测更接近体内环境条件下的持续药物释放行为与凝胶形成的基本机制。
研究团队认为,该结果对药物输送研究具有意义。P407等聚合物胶束被广泛探索用于多类新型药物载体,包括多种现代抗癌与抗炎药物。厘清盐类与离子对胶束相互作用的影响,有助于设计在体温下更稳定、且药物释放更可预测的配方。研究还显示,基于实验的量化路径可用于澄清复杂软物质体系中的相互作用与物理机制,为纳米科学走向实际应用提供支撑。












